

Cobertura especial coronavirus
Autorizan tercera dosis de Pfizer para menores de 15 años
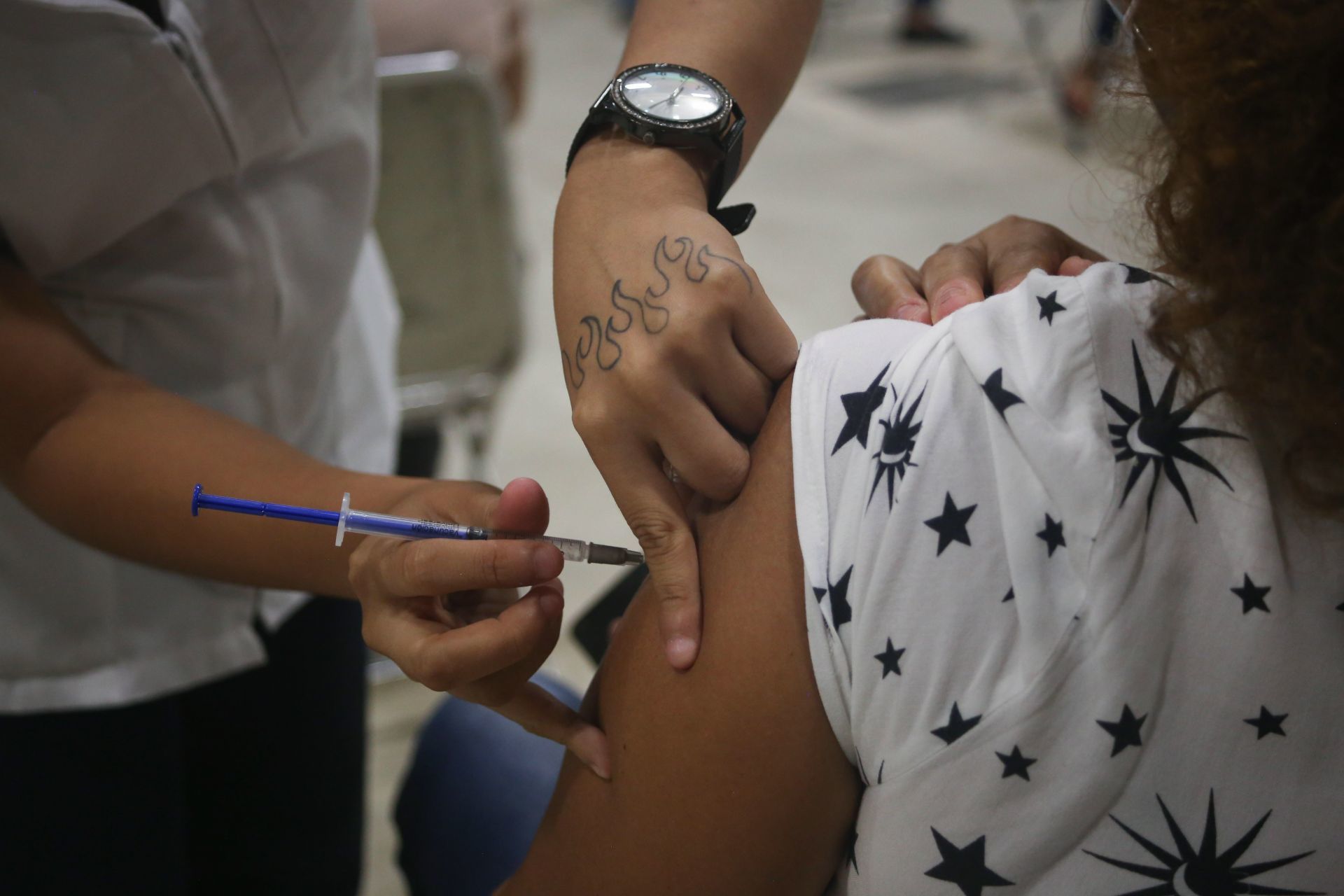
Estados Unidos.— La Administración de Alimentos y Medicamentos de Estados Unidos autorizó el uso de una tercera dosis de la vacuna contra el Covid-19 de Pfizer y BioNTech para menores entre 12 y 15 años.
De esta forma, Pfizer redujo el tiempo de todas las vacunas de refuerzo a 5 meses desde los 6 meses posteriores al fin del programa de vacunación inicial.
Asimismo autorizó una tercera dosis en niños de 5 a 11 años que estén inmunodeprimidos.
Las pruebas de laboratorio han demostrado que dos dosis de las vacunas de Pfizer-BioNTech y Moderna generan una baja respuesta inmunitaria contra Ómicron, mientras que las dosis de refuerzo son más protectoras contra la nueva variante.
LEE AMLO adelanta que aumentarán contagios de Covid-19
Cabe recordar que el 26 de noviembre de 2021, la Organización Mundial de la Salud (OMS), siguiendo el consejo del Grupo Consultivo Técnico sobre la Evolución del Virus SARS-CoV-2- en inglés, clasificó la variante B.1.1.529 de este virus como variante preocupante. Además, decidió denominarla con la letra griega Ómicron.
La decisión de considerar preocupante esta variante se basó en la evidencia presentada al Grupo Consultivo Técnico, que indica que presenta varias mutaciones que podrían afectar a las características del virus, por ejemplo, la facilidad para propagarse o la gravedad de los síntomas que causa. A continuación se resumen los conocimientos actuales a este respecto.
Conocimientos sobre la variante Ómicron
En Sudáfrica y en todo el mundo, los investigadores están realizando estudios para conocer mejor muchos aspectos de la variante Ómicron y continuarán informando de los resultados que obtengan a medida que estén disponibles.
Transmisibilidad: todavía no está claro si, con respecto a otras variantes, como la delta, la variante Ómicron es más transmisible (es decir, si se propaga con mayor facilidad de una persona a otra). El número de personas que han dado positivo en las pruebas de detección ha aumentado en las zonas de Sudáfrica afectadas por esta variante, pero se están realizando estudios epidemiológicos para determinar si ese aumento se debe a esta variante o a otros factores.
Eficacia protectora de la infección previa por el SARS-CoV-2
Los datos preliminares indican que, en comparación con otras variantes preocupantes, el riesgo de reinfección por la variante Ómicron puede ser mayor (es decir, las personas que han tenido COVID-19 antes podrían infectarse de nuevo por esta variante con más facilidad). De todos modos, la información es todavía limitada. En los próximos días y semanas tendremos más datos a este respecto.
ebv
Dejanos un comentario:
Cobertura especial coronavirus
Cofepris avala tratamiento oral de Pfizer para Covid-19
Podría ser comercializado

Ciudad de México.— La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) avaló el tratamiento antiviral oral contra el Sars-Cov 2 de Pfizer.
El Comité de Moléculas Nuevas de la Comisión Federal emitió una opinión favorable para dicho tratamiento contra Covid-19.
Hasta el momento, el tratamiento tiene la aprobación para su uso de emergencia en el país.
Sin embargo, la empresa farmacéutica busca la comercialización en todo el país a través de la obtención del registro sanitario ante la Cofepris.
Te recomendamos leer: Pirola en aumento; senadores solicitan informe de variante de Covid-19
Pfizer señaló que el fármaco oral beneficiará principalmente a personas mayores de 50 años para evitar secuelas graves por la enfermedad.
“La opinión emitida por el Comité de Cofepris es, definitivamente, un paso adelante en el cuidado y protección de la población dado que necesitamos todas las herramientas que tengamos a nuestro alcance para disminuir los riesgos del Covid-19, sobre todo en personas mayores de 50 años y con factores de riesgo, quienes continúan siendo las más susceptibles de cuadros graves y hospitalización”, señaló Daniel Bustos, director médico de Pfizer.
Tras la opinión favorable para el tratamiento de Pfizer, la Cofepris deberá anunciar en las siguientes semanas si le concede el registro sanitario a Pfizer.
JAHA

Ciudad de México.— Un nuevo anticuerpo desarrollado en laboratorio logra bloquear todas las variantes del SARS-CoV-2, incluido Omicron y sus subvariantes.
El estudio realizado por expertos españoles, trabaja con un anticuerpo monoclonal. Esta es una proteína del sistema inmunitario desarrollada en el laboratorio, bautizado como 17T2.
El aislamiento del nuevo anticuerpo fue posible gracias a las muestras de sangre de un paciente infectado por el SARS-CoV-2 en marzo de 2020.
A partir de estas muestras, se seleccionaron algunos linfocitos B, las células de la sangre encargadas de producir los anticuerpos.
Te recomendamos: Cadena de farmacias ofrece vacunas contra Covid a menos de mil pesos
Se escogieron aquellos que generaban anticuerpos específicos contra la proteína de la espícula, que es la que permite al virus SARS-CoV-2 infectar las células humanas.
Mediante técnicas de ingeniería genética, el personal investigador reprodujo estos anticuerpos en el laboratorio, en fase preclínica de la investigación.
Los científicos evaluaron in vitro su actividad neutralizante, es decir, su capacidad de unirse al virus y bloquearlo, ante las diferentes variantes del SARS-CoV-2.
Así, los investigadores pudieron seleccionar el anticuerpo que conseguía neutralizarlas todas, incluyendo XBB.1.16 y BA.2.86.
Los investigadores analizaron también en un modelo de ratón no solo la capacidad terapéutica del anticuerpo, sino también la capacidad preventiva.
Descubrieron que reduce de forma significativa las lesiones en los pulmones y la carga viral.
Antes de poder aplicarlo en pacientes habrá que llevar a cabo un ensayo clínico en humanos y, de momento, hay una patente europea activa asociada a este proyecto.
JAHA
Cobertura especial coronavirus
Cofepris avala uso de emergencia de Vacuna Patria
Se usará en personas mayores de 18 años con inmunidad previa
Ciudad de México.— El Comité de Moléculas Nuevas de la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) aprobó el uso de emergencia de la vacuna Patria contra Covid-19.
El inmunológico del laboratorio Avi-Mex, para utilizarse en mayores de 18 años, con inmunidad previa.
En reunión extraordinaria, el biológico fue evaluado por expertos, quienes determinaron que la vacuna mexicana es segura y sirve como refuerzo.
El doctor Arturo Reyes Sandoval, miembro del Comité de Moléculas Nuevas, refirió que la evidencia demuestra que la vacuna es segura.
Que no se te pase: Dos Bocas trabajará a máxima capacidad el 28 de febrero: AMLO
En tanto, la doctora Lena Ruiz Azuara dijo que la evidencia de seguridad de la vacuna Patria es factible. Sin embargo, debe darse seguimiento a las personas que participaron en los estudios.
Mientras, el doctor Miguel Ángel Jorge Guevara consideró que es una vacuna segura, y los datos de los estudios presentados por Avi-Mex lo sustentan.
La doctora Rosana Pelayo Camacho aseguró que la presentación de la vacuna la hará accesible, y dará protección a la población a largo plazo.
Cofepris confirmó que pronto publicarán los estudios clínicos de la fase II y la fase II-III.
Los análisis de la vacuna patria tuvieron resultados favorables en ratones, hámsters, cerdos y ratas.
También realizaron pruebas en personas que no tenían ninguna vacuna contra SARS-CoV-2, y obtuvieron el mismo resultado, señalaron.
JAHA
Cobertura especial coronavirus
Vacuna de Moderna ya se comercializa en México
Se une a la de Pfizer como biológico comercializado

Ciudad de México.— La vacuna actualizada contra Covid-19 de Modera aprobada por la Organización Mundial de la Salud (OMS), comenzó a comercializarse en las farmacias de México.
El biológico se encuentra disponible desde el pasado 16 de enero y se une a la vacuna de Pfizer, que se comercializa desde diciembre.
Además, el gobierno mexicano suministra por su parte la rusa Sputnik y la cubana Abdala, ambas sin el aval de la OMS.
Que no se te pase: Hospitales Covid-19 capitalinos no están saturados: Sedesa
Asofarma, el representante legal en México de Moderna, explicó que la fórmula que se vende presenta respuesta inmune a las variantes circulantes, incluyendo la JN.1.
La Comisión Federal para la Protección Contra Riesgos Sanitarios (Cofepris) avaló el registro sanitario de la vacuna de Moderna el pasado 7 de diciembre.
Esto permitió su comercialización en el sector privado.
José Miguel Fonken Quiroga, director general de Asofarma, dijo que la vacuna se distribuirá a través de una red de vacunación establecida en México que incluye los sectores público y privado.
Así, estará disponible en centros de vacunación, consultorios médicos, hospitales y farmacias y puede utilizarse en personas de seis meses de edad en adelante.
“La vacuna es accesible y ofrece una respuesta inmune robusta contra las variantes circulantes dominantes”, señaló Fonken Quiroga en un comunicado.
La farmacéutica no reveló el costo de la vacuna, pero sería similar al que tiene el biológico de Pfizer que es de 848 pesos promedio.
JAHA
-
CDMXhace 2 días
Arzobispo Aguiar Retes reconoce la unidad espiritual entre los seres humanos
-
Méxicohace 2 días
63% de las presas con menos de la mitad de su capacidad pese a lluvias: SMN
-
Futbol Internacionalhace 2 días
Santiago Giménez es sondeado por cinco grandes de Europa
-
Méxicohace 2 días
“Marcha por la Vida”: Agustín Laje llama a la defensa de los no nacidos en México

































