Cobertura especial coronavirus
Ssa debe informar promedio de contagios que genera paciente con Covid
Ciudad de México.— El Instituto Nacional de Transparencia, Acceso a la Información y Protección de Datos Personales (INAI) instruyó a la Secretaría de Salud dar a conocer el número básico de reproducción de la enfermedad Covid-19 especificando la cobertura temporal y geográfica.
“Esa respuesta no sólo es legítima y urgente para quien la pidió, sino que es importante para México entero. Porque con la variable R se puede reconocer si se hizo lo adecuado”, afirmó el Comisionado Presidente del INAI, Francisco Javier Acuña Llamas.
Acuña Llamas explicó que el factor o variable R corresponde al promedio de contagios que se producen a partir de una persona enferma. “Por ejemplo, en Wuhan, China, donde inició esta pesadilla mundial del Covid-19, el promedio de contagio fue de 2 a 2.5”.
El solicitante de la información especificó que, en caso de contar con más de un punto en el tiempo, sobre el número básico de reproducción, requería el más reciente y los puntos anteriores para conocer su evolución. Por otra parte, señaló que, en caso de existir más de un dato de referencia geográfica, se le proporcionaran el nacional y los de las entidades federativas.
La Secretaría de Salud, a través de la Dirección General de Epidemiología, remitió un vínculo electrónico para consultar la información solicitada; mientras que la Unidad de Transparencia indicó que lo requerido es de carácter público y se encuentra en el micrositio electrónico https://coronavirus.gob.mx; además, diariamente, se actualiza el Comunicado Técnico Diario y las conferencias del reporte diario de “Covid-19” se transmiten en cadena nacional.
Inconforme, el solicitante interpuso un recurso de revisión ante el INAI, mediante el cual manifestó que la información entregada no corresponde con lo solicitado; pues es una respuesta genérica, que no muestra las cifras de “R0” o “Rt”; además de que el vínculo electrónico proporcionado por la Dirección General de Epidemiología es un manual sobre influenza de 2014.
En alegatos, la Secretaría de Salud declaró la inexistencia de la información relacionada con la variable “R0 de Covid-19”, aclarando que no se ha realizado ninguna medición de este factor.
En una consulta del micrositio electrónico https://coronavirus.gob.mx, el INAI corroboró que no existe información sobre el número básico de reproducción para el Covid-19; además, la sola mención de un vínculo electrónico sin el detalle de los pasos a seguir para consultar la información requerida, no satisface el derecho de acceso a la información en cuestión. Por otra parte, fue imposible acceder al vínculo electrónico proporcionado por la Dirección General de Epidemiología.
Sobre la inexistencia de la información, declarada por la Secretaría de Salud vía alegatos, el Instituto señaló; el 28 de mayo de 2020, el subsecretario, Hugo López Gatell, señaló que existe una medida denominada “R”. Una variable muy importante en epidemiología matemática.
El 13 de julio de 2020, durante el informe diario vespertino sobre el Covid-19 en México, López Gatell presentó el número básico de reproducción; esto con respecto al periodo transcurrido del 28 de mayo al 26 de junio de 2020.
Por lo anterior, el Pleno del INAI revocó la respuesta de la Secretaría de Salud y le instruyó informar al solicitante el número básico de reproducción para la enfermedad Covid-19; especificar la cobertura temporal y geográfica detallando los datos a nivel nacional y de las entidades federativas.
LEE Raquel es la única en el país diagnosticada con la enfermedad ECHS1
ebv
Cobertura especial coronavirus
Vacuna de AstraZeneca se deja de comercializar por trombosis
En Europa
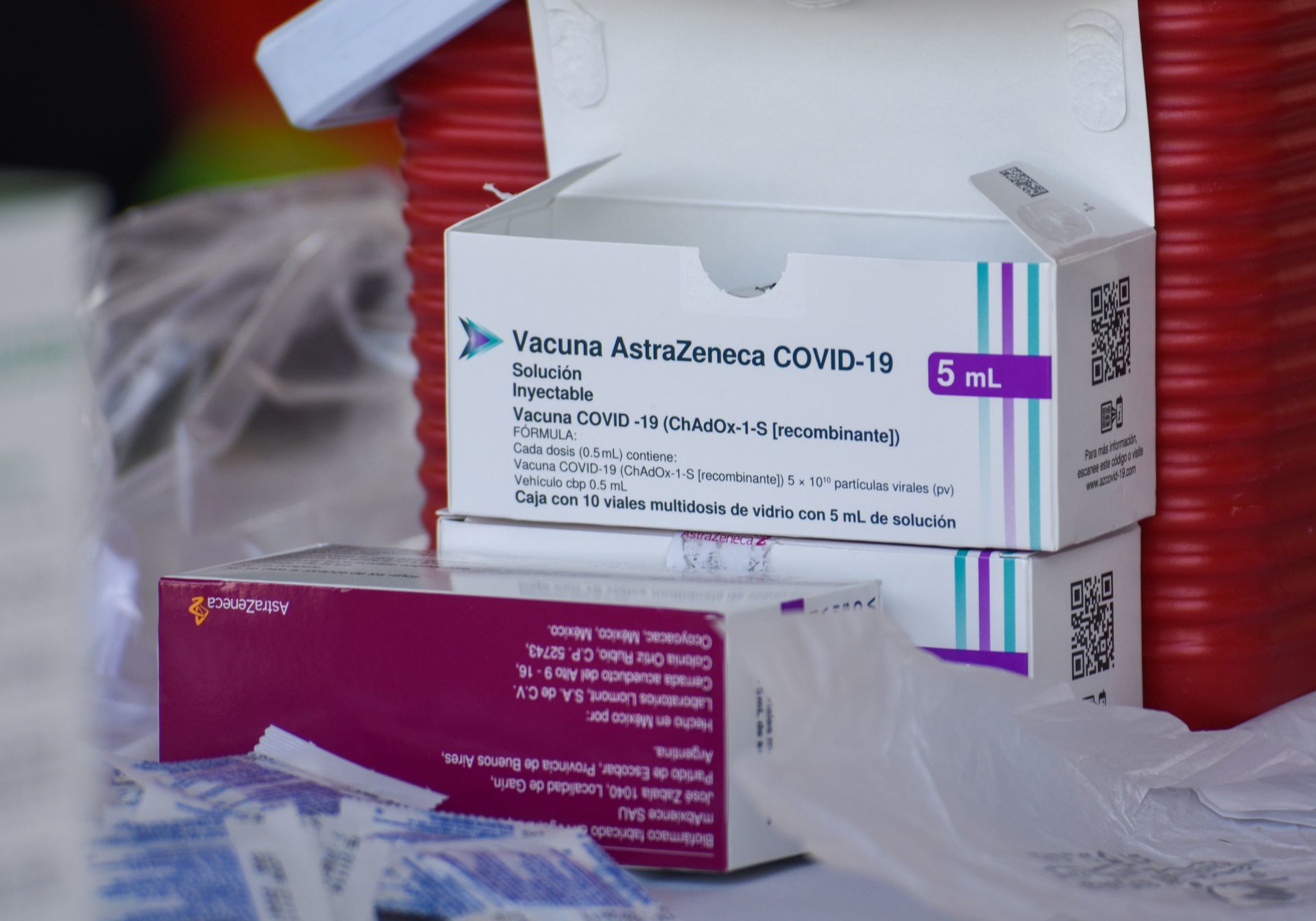
Madrid.— Desde este martes, la vacuna contra Covid-19 que lleva por nombre Vaxzeria desarrollada por AstraZeneca, dejó de comercializarse en Europa.
Lo anterior, luego de que la Comisión Europea validara una petición de la farmacéutica de retirar el biológico el pasado 5 de marzo.
La semana pasada, la compañía farmacéutica AstraZeneca admitió por primera vez que su vacuna contra el coronavirus podía provocar efectos secundarios como la trombosis.
Dicho efecto que ya se notificó en plena pandemia y que provocó la limitación de dicho vial durante el año 2021.
Sobre el tema: AstraZeneca reconoce que vacuna anticovid puede causar trombosis
Se han presentado 51 casos ante el Tribunal Superior, y las víctimas y sus familiares en duelo piden daños y perjuicios por un valor estimado de hasta 100 millones de libras esterlinas.
La farmacéutica justificó la retirada de la vacuna contra Covid-19 por la falta de demanda y por el excedente de vacunas disponibles en el mercado.
“Dado que se han desarrollado múltiples vacunas actualizadas para variantes de Covid-19, ahora hay un excedente de vacunas disponibles. Esto ha provocado una disminución en la demanda de Vaxzervria, que ya no se fabrica ni suministra”, indica en un comunicado.
La vacuna de AstraZeneca contra Covid-19 fue la tercera en recibir la aprobación de los reguladores europeos, después de las elaboradas por Pfizer/BioTech y Moderna.
JAHA
Cobertura especial coronavirus
AstraZeneca reconoce que vacuna anticovid puede causar trombosis
Se han presentado 51 casos
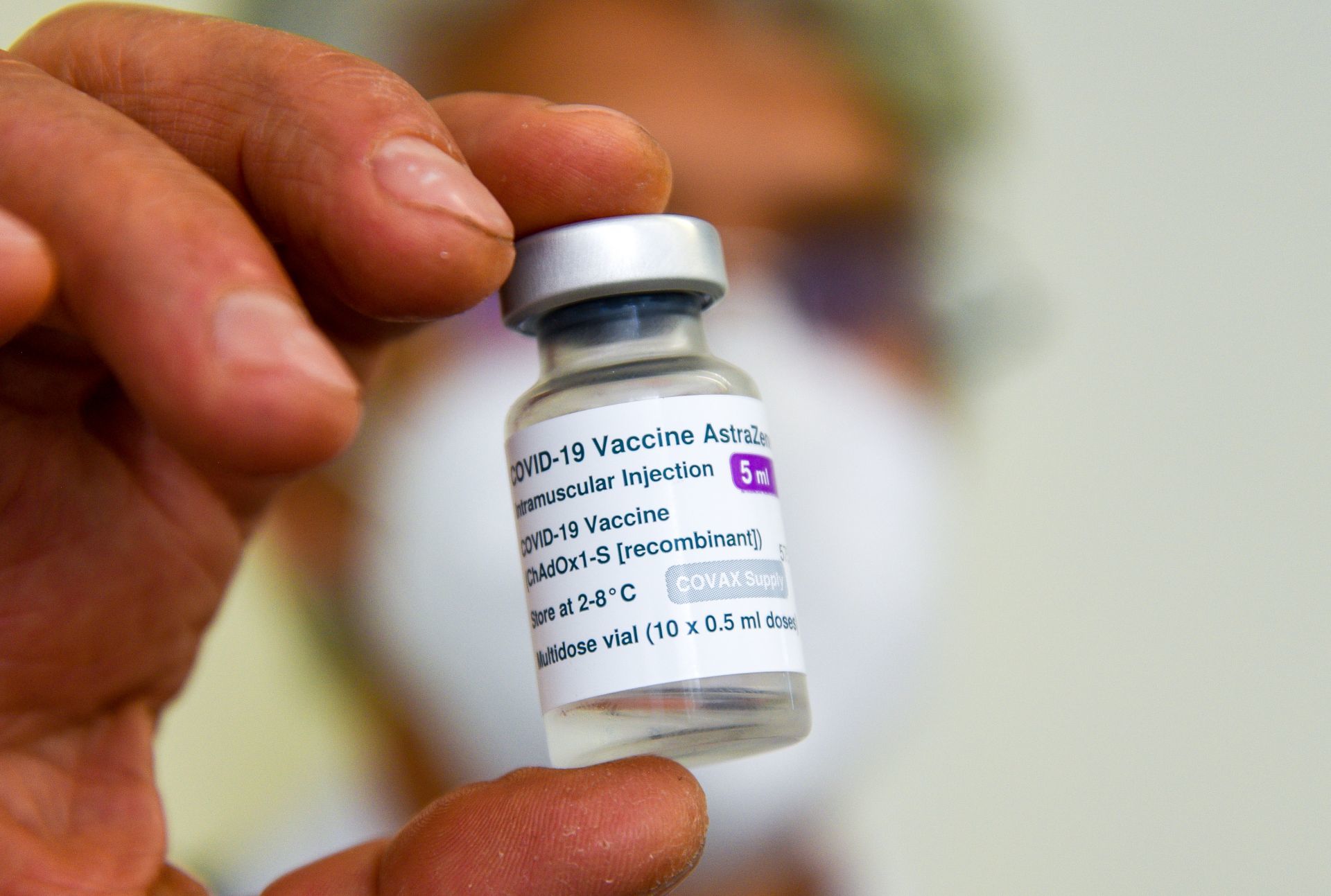
Londres.— AstraZeneca reconoció públicamente, por primera vez en un tribunal que su vacuna contra Covid-19 puede tener un efecto secundario extremadamente raro.
Sin embargo, de presentarse puede ser mortal, pues se puede desencadenar el síndrome de trombosis con trombocitopenia” (TTS).
Usuarios emprendieron en Reino Unido una acción colectiva contra el gigante farmacéutico y su vacuna para el Covid-19, desarrollada junto con la Universidad de Oxford.
Según The Telegraph, AstraZeneca rechazó las demandas, pero aceptó, en un documento legal que su vacuna “puede, en casos muy raros, causar TTS”.
Más para leer: Papa Francisco: “Cambio climático amenaza a Venecia”
Hasta ahora, se han presentado 51 demandas ante el Tribunal Supremo británico. En ellas, las víctimas y sus familiares reclaman una indemnización por daños y perjuicios estimada en 100 millones de libras esterlinas.
No es la única demanda que enfrenta AstraZeneca. En Alemania, un tribunal ordenó a la empresa revelar los datos sobre casos de trombosis posiblemente relacionados con su vacuna.
Lo anterior se da luego de que una mujer de 33 años que reclama una indemnización de 250 mil euros por los dolores que tuvo.
Además de otra de 17 mil 200 euros por concepto de ingresos que dejó de percibir y hasta 600 mil euros por futuras limitaciones.
Por ello, las autoridades solicitaron que AstraZeneca revele los casos de trombosis sufridos por gente que haya recibido la vacuna entre el 27 de diciembe de 2020 y el 19 de febrero de 2024.
La vacuna, según el tribunal, puede en principio favorecer la trombosis. El fabricante ya ha ofrecido información parcial que ahora deberá completar.
JAHA
Cobertura especial coronavirus
Cofepris avala tratamiento oral de Pfizer para Covid-19
Podría ser comercializado

Ciudad de México.— La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) avaló el tratamiento antiviral oral contra el Sars-Cov 2 de Pfizer.
El Comité de Moléculas Nuevas de la Comisión Federal emitió una opinión favorable para dicho tratamiento contra Covid-19.
Hasta el momento, el tratamiento tiene la aprobación para su uso de emergencia en el país.
Sin embargo, la empresa farmacéutica busca la comercialización en todo el país a través de la obtención del registro sanitario ante la Cofepris.
Te recomendamos leer: Pirola en aumento; senadores solicitan informe de variante de Covid-19
Pfizer señaló que el fármaco oral beneficiará principalmente a personas mayores de 50 años para evitar secuelas graves por la enfermedad.
“La opinión emitida por el Comité de Cofepris es, definitivamente, un paso adelante en el cuidado y protección de la población dado que necesitamos todas las herramientas que tengamos a nuestro alcance para disminuir los riesgos del Covid-19, sobre todo en personas mayores de 50 años y con factores de riesgo, quienes continúan siendo las más susceptibles de cuadros graves y hospitalización”, señaló Daniel Bustos, director médico de Pfizer.
Tras la opinión favorable para el tratamiento de Pfizer, la Cofepris deberá anunciar en las siguientes semanas si le concede el registro sanitario a Pfizer.
JAHA

Ciudad de México.— Un nuevo anticuerpo desarrollado en laboratorio logra bloquear todas las variantes del SARS-CoV-2, incluido Omicron y sus subvariantes.
El estudio realizado por expertos españoles, trabaja con un anticuerpo monoclonal. Esta es una proteína del sistema inmunitario desarrollada en el laboratorio, bautizado como 17T2.
El aislamiento del nuevo anticuerpo fue posible gracias a las muestras de sangre de un paciente infectado por el SARS-CoV-2 en marzo de 2020.
A partir de estas muestras, se seleccionaron algunos linfocitos B, las células de la sangre encargadas de producir los anticuerpos.
Te recomendamos: Cadena de farmacias ofrece vacunas contra Covid a menos de mil pesos
Se escogieron aquellos que generaban anticuerpos específicos contra la proteína de la espícula, que es la que permite al virus SARS-CoV-2 infectar las células humanas.
Mediante técnicas de ingeniería genética, el personal investigador reprodujo estos anticuerpos en el laboratorio, en fase preclínica de la investigación.
Los científicos evaluaron in vitro su actividad neutralizante, es decir, su capacidad de unirse al virus y bloquearlo, ante las diferentes variantes del SARS-CoV-2.
Así, los investigadores pudieron seleccionar el anticuerpo que conseguía neutralizarlas todas, incluyendo XBB.1.16 y BA.2.86.
Los investigadores analizaron también en un modelo de ratón no solo la capacidad terapéutica del anticuerpo, sino también la capacidad preventiva.
Descubrieron que reduce de forma significativa las lesiones en los pulmones y la carga viral.
Antes de poder aplicarlo en pacientes habrá que llevar a cabo un ensayo clínico en humanos y, de momento, hay una patente europea activa asociada a este proyecto.
JAHA
-

 Historias que Conectanhace 3 días
Historias que Conectanhace 3 díasLa vida suena; niña de 12 años vence al cáncer
-

 Historias que Conectanhace 3 días
Historias que Conectanhace 3 díasEl mediocampista que jugó con un milagro bajo el corazón: la fe que sostuvo a Alberto García Aspe
-

 Culturahace 3 días
Culturahace 3 díasLa Virgen de Guadalupe y las múltiples advocaciones marianas
-

 Méxicohace 3 días
Méxicohace 3 díasEducación básica tendrá nuevos protocolos obligatorios para la entrega y recepción de menores